Bioscience Institute
Pionieri nelle Tecnologie Avanzate per la Longevità
Dal 2007, Bioscience Institute si è affermato come leader internazionale nei servizi di biologia cellulare e molecolare, operando piattaforme di sequenziamento all’avanguardia e laboratori GMP per la produzione cellulare in Italia e negli Emirati Arabi Uniti. Come spin-off dell’Università di Roma, Bioscience Institute è specializzato in Genomica per il sequenziamento del cfDNA, nella coltura di cellule staminali mesenchimali e di esosomi per terapie personalizzate avanzate, fondamentali per contrastare i processi degenerativi causati dall’invecchiamento o da condizioni patologiche. Le procedure di estrazione, espansione e conservazione di cellule staminali ed esosomi vengono eseguite nei laboratori di Dubai e d’Italia, mentre le attività di Genomica hanno sede a Roma.
I servizi di Bioscience Institute sono unici, poiché offrono le più avanzate terapie con cellule staminali ed esosomi per difetti legati all’età. Bioscience Institute ha sviluppato protocolli rivoluzionari per il sequenziamento del DNA circolante, concepiti per identificare i fattori alla base dell’invecchiamento e delle patologie correlate. Questa innovazione consente una medicina preventiva di precisione, personalizzata sulle esigenze del singolo individuo. La tecnologia proprietaria del centro è in grado di rilevare minime variazioni genetiche che contribuiscono alla senescenza cellulare e al degrado tissutale, permettendo interventi precoci prima della comparsa dei sintomi clinici.
La combinazione di due aree di eccellenza – cellule staminali e sequenziamento del cfDNA – ha posizionato Bioscience Institute come azienda leader nel settore della longevità.
GENOTOSSICITÀ
Il principale motore dell’invecchiamento
BIOXPACE è un metodo innovativo sviluppato da Bioscience Institute, incentrato sullo studio dell’accumulo di genotossicità e sulla gestione dell’esaurimento delle cellule staminali negli organi e nei tessuti umani. Questo protocollo è stato ideato non solo per prolungare la durata della vita, ma anche per migliorarne la qualità, offrendo la possibilità di invecchiare in modo più sano.
L’invecchiamento biomolecolare è influenzato principalmente dalle interazioni tra geni e fattori ambientali che provocano danni al DNA. Con l’avanzare dell’età, l’efficienza dei meccanismi di riparazione del DNA, noti come DNA Damage Response, diminuisce. Ogni giorno, il DNA subisce tra i 10.000 e i 20.000 eventi di danno, la maggior parte dei quali viene efficacemente riparata dai meccanismi cellulari. Tuttavia, i danni non riparati tendono ad accumularsi, portando a una condizione di genotossicità che compromette la stabilità genomica e accelera i processi di invecchiamento.

CATTIVE ABITUDINI CHE FAVORISCONO LA GENOTOSSICITÀ
L’approccio proposto dal protocollo BioXpace consente di sviluppare strategie mediche personalizzate finalizzate a potenziare i meccanismi di riparazione del DNA e a prevenire l’accumulo di danni significativi, alla base della genotossicità.
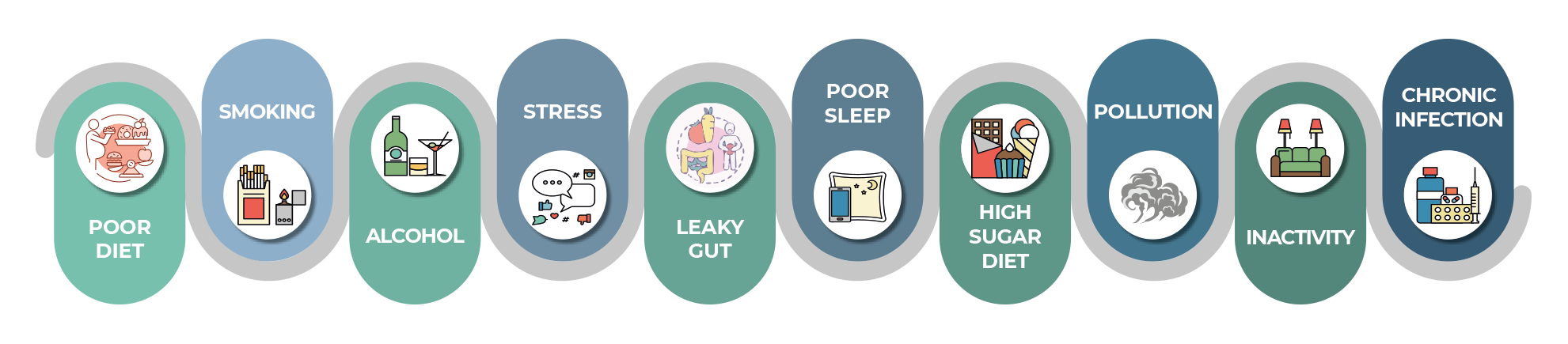
Nel corso della vita, le condizioni fisiologiche cambiano a causa dell’accumulo di danni genotossici derivanti dall’inquinamento ambientale, dalle scelte di stile di vita e dai processi cellulari naturali.
Questo accumulo di genotossicità aumenta il numero di cellule senescenti, che perdono la capacità di proliferare e rilasciano segnali infiammatori, dando origine a un’infiammazione sistemica.
Il sistema immunitario, che normalmente contribuisce a ripristinare l’equilibrio eliminando le cellule senescenti per ridurre l’infiammazione, sotto stress continuo diventa disfunzionale e non riesce più a svolgere adeguatamente il proprio ruolo.
L’efficacia del sistema immunitario è inoltre strettamente legata all’equilibrio del microbioma intestinale, che ne influenza le capacità protettive.
GENOTOSSICITÀ
LA CAUSA DEI PROCESSI DEGENERATIVI
La causa dei processi degenerativi è il progressivo accumulo di danni al DNA (provenienti da fonti fisiche, chimiche e da radiazioni) che non possono essere riparati e che provocano l’invecchiamento riducendo la concentrazione e la funzionalità delle cellule staminali nei tessuti e negli organi, compromettendo le capacità rigenerative dell’organismo e favorendo i processi di invecchiamento.
Mutazioni Somatiche Passeggere
Cicatrici Genetiche Silenziose
Numerose e per lo più neutre alterazioni del DNA che si accumulano con l’età
Registro dei Danni
Costituiscono una traccia delle esposizioni subite nel corso della vita a influenze genotossiche
Impatto Collettivo
Compromettono le funzioni cellulari e possono portare a disfunzioni tissutali o a un declino delle funzionalità degli organi legato all’età
Predisposizione Genetica Ereditata
Cosa misura
Analisi delle mutazioni germinali ereditarie che predispongono a malattie correlate all’età.
Ruolo nell’invecchiamento
Difetti germinali nei meccanismi di riparazione del DNA causano sindromi da invecchiamento e influenzano i sistemi di mantenimento dell’organismo.
Rilevanza clinica
Contribuisce a personalizzare la valutazione e gli interventi. Gli individui necessitano di una diversa frequenza di monitoraggio in base alla predisposizione.
Genotossicità e Stress Ossidativo
Danno Misurabile
Questo test valuta l’ossidazione delle basi del DNA, i carbonili proteici e i perossidi lipidici.
Motore dell’Invecchiamento
Le specie reattive dell’ossigeno (ROS) provocano danni cumulativi al DNA, alle proteine e alle membrane cellulari. Un elevato carico di stress ossidativo significa che il “motore dell’invecchiamento” sta girando al massimo.
Collegamento con le Malattie
I livelli individuali di stress ossidativo offrono un’indicazione di quanto aggressivamente stiano avanzando i processi fondamentali dell’invecchiamento.
Cellule Senescenti: le “Cellule Zombie” dell’Invecchiamento
Le cellule senescenti secernono fattori infiammatori noti come SASP (Senescence-Associated Secretory Phenotype). Il SASP genera un’infiammazione “sterile”, che accelera l’invecchiamento e favorisce l’insorgenza di malattie in diversi organi, come fegato e reni, dove contribuisce allo sviluppo di fibrosi e insufficienza d’organo.
Quando la rimozione immunitaria risulta inefficace a causa di uno squilibrio del sistema immunitario, le cellule senescenti persistono e si diffondono nell’organismo, promuovendo un’infiammazione cronica di basso grado e i processi degenerativi correlati.
Deficienza del Sistema Immunitario & Sorveglianza Senolitica
INVECCHIAMENTO DELLE CELLULE IMMUNITARIE
Con l’avanzare dell’età, le cellule immunitarie mostrano segni di esaurimento e disfunzione. Ciò include la riduzione dei linfociti T naïve, l’accumulo di cellule T in fase avanzata di differenziazione e la diminuzione delle risposte proliferative agli stimoli, un insieme di fenomeni noto come immunosenescenza.
FUNZIONE SENOLITICA
Le cellule Natural Killer (NK) svolgono un ruolo cruciale nell’eliminazione delle cellule senescenti. Le cellule NK riconoscono i segnali di “allarme” sulla superficie delle cellule senescenti e le distruggono. Questa funzione di “pulizia” previene l’accumulo di cellule danneggiate che potrebbero contribuire a disfunzioni tissutali.
DNA DAMAGE RESPONSE
IL GUARDIANO GENOMICO CONTRO L’INVECCHIAMENTO
Il suo obiettivo è riparare accuratamente il DNA e ripristinarne la sequenza originale, ma questo processo non è infallibile. Errori nella riparazione portano a mutazioni somatiche — cambiamenti irreversibili che causano INSTABILITÀ GENOMICA e GENOTOSSICITÀ.
Potenziare la DNA Damage Response: una strategia per la longevità
Monitoraggio dell’efficienza
Sistemi come HELIXBALANCE valutano i meccanismi di riparazione del DNA e forniscono informazioni fondamentali sul mantenimento della stabilità genomica.
Intervento mirato
Correggere le carenze nei sistemi di riparazione può prevenire l’insorgenza e la progressione dell’invecchiamento e delle malattie correlate all’età.
Approccio preventivo
Rafforzare la DDR rappresenta una strategia vitale per promuovere la salute a lungo termine, con l’obiettivo di prevenire l’accumulo di danni molecolari.
L'impatto nascosto delle micro e nanoplastiche (MNP)
Citochine Pro-Infiammatorie
IL-17A – TNF-α – IL-6 – IL-4 – IFN-γ – IL-12 – IL-10 – Proteina C-Reattiva
Principali citochine infiammatorie prodotte dalle cellule immunitarie e da quelle senescenti. Provocano danni al DNA attraverso la generazione di ROS e sopprimono l’attività della telomerasi. Sono citochine tipiche del SASP, fortemente associate a fragilità e mortalità. Ostacolano la riparazione del DNA e mantengono lo stato di senescenza nelle cellule vicine.
Equilibrio del Microbioma Intestinale
L’Asse Intestino-Sistema Immunitario-Cervello
Cambiamenti del microbioma
Con l’avanzare dell’età, i batteri benefici diminuiscono mentre aumentano le specie pro-infiammatorie. Questo squilibrio può ridurre la produzione di metaboliti utili, come gli acidi grassi a catena corta, e aumentare la produzione di composti infiammatori.
Disfunzione della barriera intestinale
Un microbioma disbiotico indebolisce la barriera intestinale, portando al cosiddetto “leaky gut”. Ciò consente a prodotti batterici come il lipopolisaccaride (LPS) di entrare in circolazione, innescando un’infiammazione sistemica.
Attivazione immunitaria
LPS e altri composti microbici attivano le cellule immunitarie, stimolando la produzione di citochine pro-infiammatorie. Questa attivazione immunitaria cronica contribuisce al fenomeno dell’inflammaging.
Effetti sistemici
I segnali infiammatori si diffondono in tutto l’organismo, influenzando organi distanti, incluso il cervello. Ciò può contribuire alla neuroinfiammazione e potenzialmente accelerare malattie neurodegenerative come l’Alzheimer.
VALUTAZIONE DELLA GENOTOSSICITÀ
PREDISPOSIZIONE GENETICA LEGATA ALL’ETÀ – MUTAZIONI GERMINALI
Comprendere la predisposizione genetica individuale allo sviluppo di malattie correlate all’età guida misure preventive personalizzate per ridurre i rischi associati.
INSTABILITÀ GENOMICA – MUTAZIONI SOMATICHE DRIVER DEL CANCRO
Identifica l’accumulo progressivo di mutazioni somatiche in geni che guidano attivamente lo sviluppo del cancro e contribuiscono all’instabilità genomica complessiva.
INSTABILITÀ GENOMICA – MUTAZIONI SOMATICHE PASSENGER
Le mutazioni “passeggere” sono segni di instabilità genomica e riflettono la storia dell’esposizione della cellula a stress genotossici. Permettono di valutare l’impatto dei fattori genotossici ambientali ed endogeni.
EMATOPOIESI CLONALE DI POTENZIALE INDETERMINATO (CHIP)
Associata a un aumento del rischio di tumori ematologici, malattie cardiovascolari e condizioni legate all’età. La presenza di CHIP è un indicatore di instabilità genomica nelle cellule ematopoietiche.
ANALISI E QUANTIFICAZIONE DI MICRO/NANOPLASTICHE
Le micro/nanoplastiche alterano i processi biologici imitando o interferendo con gli ormoni, causando infiammazione o persino trasportando altre tossine all’interno delle cellule.

EFFICIENZA DELLA DNA DAMAGE RESPONSE
CELLULE SENESCENTI E ACCUMULO DEL FENOTIPO SECRETORIO ASSOCIATO ALLA SENESCENZA (SASP)
Senescent cells lead to tissue dysfunction and promote chronic diseases associated with aging. Identifying the accumulation is critical for implementing senolytic therapies that clear the cells.
GENOTOSSICITÀ E STRESS OSSIDATIVO
Si riferisce al livello di danno causato da agenti genotossici, che può indurre mutazioni e invecchiamento cellulare implicato in diverse malattie degenerative.
INFIAMMAZIONE CRONICA SISTEMICA DI BASSO GRADO
Il test dei biomarcatori infiammatori aiuta a determinare l’entità dell’infiammazione e a facilitare strategie per ridurne l’impatto e gli effetti sull’invecchiamento.
DEFICIENZA DEL SISTEMA IMMUNITARIO NELLA CLEARANCE IMMUNITARIA
Valuta la capacità del sistema immunitario di ringiovanire eliminando le cellule senescenti che ne compromettono la funzione e di ridurre l’incidenza di infezioni, tumori e altre patologie correlate all’età.
EQUILIBRIO BATTERICO DEL MICROBIOMA INTESTINALE
Svolge un ruolo cruciale nella salute generale, influenzando il metabolismo, il sistema immunitario e persino le funzioni cerebrali. Uno squilibrio della flora intestinale è associato a condizioni patologiche.

GENOTOSSICITÀ – CELLULE STAMINALI – INVECCHIAMENTO
Il processo attraverso il quale l’accumulo di genotossicità porta a una riduzione della concentrazione e della funzionalità delle cellule staminali, generando condizioni che favoriscono l’invecchiamento, coinvolge diversi meccanismi biologici interconnessi.
La genotossicità si riferisce ai danni inflitti al DNA all’interno delle cellule e comporta una diminuzione della concentrazione complessiva di cellule staminali funzionali. Con il calo del numero di cellule staminali sane, diminuisce la capacità dei tessuti di rigenerarsi e ripararsi, una caratteristica tipica dei tessuti invecchiati.
Le cellule staminali che sopravvivono allo stress genotossico possono comunque subire danni sub-letali al DNA o alterazioni epigenetiche, che ne compromettono la funzionalità. Con la riduzione del pool di cellule staminali funzionali e la perdita della loro capacità rigenerativa, la funzionalità complessiva degli organi inizia a declinare.
Questo rappresenta un aspetto chiave dell’invecchiamento a livello cellulare. La diminuzione della rigenerazione tissutale efficace porta al deterioramento progressivo dei sistemi d’organo, che si manifesta con i segni fisici dell’invecchiamento e con una maggiore suscettibilità alle malattie correlate all’età.
PROPRIETÀ DELLE CELLULE STAMINALI MESENCHIMALI
I trattamenti con cellule staminali mesenchimali (MSCs) espanse rallentano i processi di invecchiamento e prevengono le malattie correlate all’età attraverso diversi meccanismi biologici e molecolari, tra cui:
- Riduzione dell’infiammazione sistemica, un fattore chiave nella patogenesi di molte malattie croniche legate all’età (come artrite, malattie cardiovascolari e diabete).
- Riparazione e rigenerazione dei tessuti danneggiati, in particolare quelli con una naturale capacità rigenerativa limitata.
- Modulazione delle risposte immunitarie, con miglioramento della funzione dei linfociti T e riduzione della frequenza di reazioni autoimmuni o condizioni infiammatorie croniche.
- Riduzione della senescenza cellulare e mantenimento dell’integrità e della funzionalità dei tessuti.
- Effetti protettivi contro lo stress ossidativo, grazie alla secrezione di molecole antiossidanti o all’attivazione di pathway antiossidanti nelle cellule ospiti.
- Promozione della formazione di nuovi vasi sanguigni per migliorare la perfusione tissutale e contribuire alla funzione e alla rigenerazione dei tessuti.
RISULTATI DELLE TERAPIE CON CELLULE STAMINALI MESENCHIMALI
Miglioramento delle prestazioni fisiche e della vitalità
Aumenta le performance fisiche e i livelli di energia.
Effetti neuroprotettivi
Migliora le funzioni cognitive e la chiarezza mentale.
Riparazione e rigenerazione dei tessuti
Favorisce la guarigione e la rigenerazione dei tessuti danneggiati.
Riduzione del declino legato all’età
Contribuisce a ridurre i segni visibili dell’invecchiamento e a sostenere la salute.
Supporto al sistema immunitario
Potenzia la protezione contro le malattie grazie alle proprietà immunomodulatorie.
Sistema cardiorespiratorio
Migliora la funzione polmonare e cardiaca, aumentando la resistenza e la capacità di recupero.
Sistema muscoloscheletrico
Riduce i tempi di recupero e potenzia le prestazioni, favorendo muscoli più forti.
Sistema circolatorio
Migliora l’elasticità dei vasi sanguigni e la circolazione periferica.
RISULTATI DELLE TERAPIE CON CELLULE STAMINALI MESENCHIMALI
Miglioramento delle prestazioni fisiche e della vitalità
Aumenta le performance fisiche e i livelli di energia.
Effetti neuroprotettivi
Migliora le funzioni cognitive e la chiarezza mentale.
Riparazione e rigenerazione dei tessuti
Favorisce la guarigione e la rigenerazione dei tessuti danneggiati.
Riduzione del declino legato all’età
Contribuisce a ridurre i segni visibili dell’invecchiamento e a sostenere la salute.
Supporto al sistema immunitario
Potenzia la protezione contro le malattie grazie alle proprietà immunomodulatorie.
Sistema cardiorespiratorio
Migliora la funzione polmonare e cardiaca, aumentando la resistenza e la capacità di recupero.
Sistema muscoloscheletrico
Riduce i tempi di recupero e potenzia le prestazioni, favorendo muscoli più forti.
Sistema circolatorio
Migliora l’elasticità dei vasi sanguigni e la circolazione periferica.
INTEGRATORI ALIMENTARI SENZA GENOTOSSICITÀ
RISCHI DEGLI INTEGRATORI ALIMENTARI STANDARD
L’industria degli integratori non è regolamentata in modo rigoroso come quella farmaceutica. Questa mancanza di controlli stringenti può consentire l’immissione sul mercato di sostanze potenzialmente dannose, non adeguatamente testate per la sicurezza, in grado di provocare danni al DNA. Gli integratori possono risultare contaminati da metalli pesanti genotossici, pesticidi o altri inquinanti durante la coltivazione, la lavorazione o il confezionamento.
INTEGRATORI ALIMENTARI SENZA GENOTOSSICITÀ
Bioscience Institute offre la possibilità di produrre integratori privi di effetti genotossici grazie al controllo dei fattori ambientali — come inquinamento, particolato, luce, temperatura e umidità — riducendo in modo significativo l’impatto dell’esposizione a contaminanti ambientali.
AFFRONTARE LA GENOTOSSICITÀ NELL’INVECCHIAMENTO
Le piante coltivate in vertical farm possono essere selezionate e ottimizzate per aumentare il contenuto nutrizionale, inclusi antiossidanti come le vitamine C ed E, che contrastano lo stress ossidativo, uno dei principali fattori di danno al DNA e invecchiamento. In questo modo si supportano i meccanismi di riparazione del DNA e la salute cellulare, riducendo potenzialmente la genotossicità.
RIDUZIONE DEI DANNI AL DNA
Gli integratori alimentari sviluppati da Bioscience Institute contribuiscono a ridurre l’accumulo di danni al DNA nel tempo, affrontando una delle principali cause dell’invecchiamento.



CLINICAL DECISION SUPPORT SYSTEM (CDSS)
Analizza i dati del paziente confrontandoli con basi di conoscenza medica per fornire raccomandazioni basate su evidenze direttamente al punto di cura. Questi sistemi guidano i clinici a seguire il flusso di lavoro suggerendo procedure diagnostiche e trattamenti.
STANDARD OPERATING PROCEDURE (SOPs)
Le Standard Operating Procedures (SOPs) guidano i professionisti sanitari attraverso protocolli consolidati. Questa standardizzazione riduce la variabilità nell’erogazione delle cure e minimizza gli errori.
DATA MANAGEMENT
Funzionalità robuste di raccolta e gestione dei dati dei pazienti assicurano che le informazioni vengano acquisite in modo accurato, archiviate in sicurezza e rese accessibili quando necessario.
COMPLIANCE
La gestione automatizzata degli accordi di qualità (Quality Agreements) e dei moduli di consenso informato garantisce una documentazione completa, riducendo al contempo il carico amministrativo.
DASHBOARD MONITORING
Dashboard interattive mostrano metriche cliniche e operative essenziali, consentendo ai professionisti di identificare trend, monitorare gli esiti e intervenire in modo proattivo.

I LIMITI DEGLI ATTUALI INTERVENTI PER LA LONGEVITÀ: AFFRONTARE I SINTOMI INVECE DELLE CAUSE
Nella ricerca di una vita più lunga e di una migliore qualità negli anni successivi, sono stati proposti e applicati numerosi interventi, come la terapia iperbarica, la crioterapia, le infusioni di varie sostanze, l’ozono, l’ossigeno e altri ancora.
Tuttavia, un’analisi critica mette in evidenza un limite fondamentale: la maggior parte di questi interventi mira alle manifestazioni visibili dell’invecchiamento piuttosto che ai suoi meccanismi biologici di base.

IL GAP BIOMOLECOLARE
Gli approcci attuali all’invecchiamento si concentrano principalmente sul sollievo sintomatico piuttosto che sull’affrontare i fattori biomolecolari fondamentali dell’invecchiamento, come l’instabilità genomica, l’accorciamento dei telomeri e le alterazioni epigenetiche.
Questi meccanismi di base, le vere e proprie “cause radice” dell’invecchiamento, accumulano danni a livello cellulare nel tempo. Gli interventi attuali possono soltanto ritardare o mitigare il declino legato all’età, senza però modificare in maniera sostanziale la traiettoria dell’invecchiamento.
Esiste quindi un divario significativo tra gli obiettivi delle terapie attuali e i meccanismi biologici alla base dell’invecchiamento, che limita l’efficacia complessiva di tali approcci, indipendentemente dall’aderenza o dall’implementazione precoce.
Per realizzare progressi concreti nella ricerca sulla longevità, è necessario spostare l’attenzione verso interventi che agiscono direttamente su questi meccanismi cellulari dell’invecchiamento, attraverso metodiche genetiche, epigenetiche o farmacologiche avanzate.

